Precisare diagnos möjlig med analys av hela arvsmassan
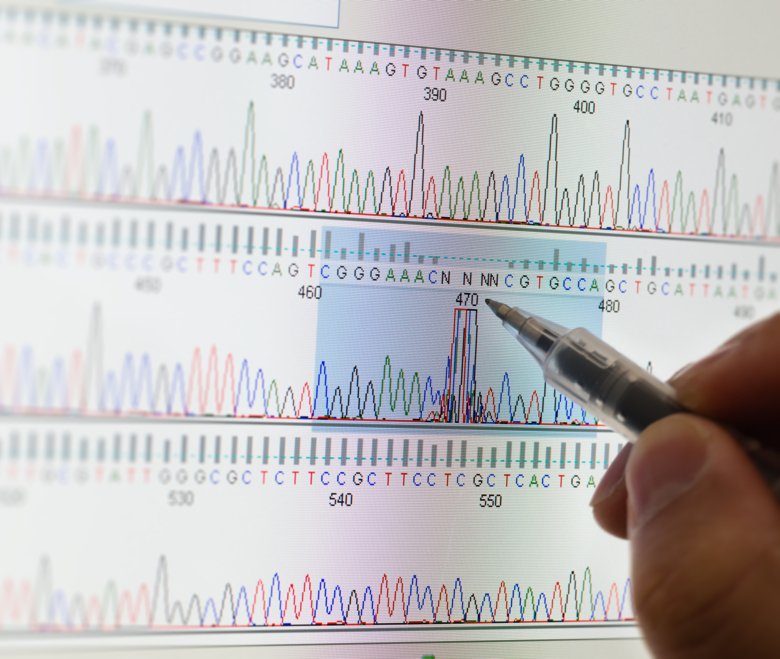
Fler än 1 200 personer med sällsynta sjukdomar har hittills fått en genetisk diagnos tack vare integrering av storskalig genomik i sjukvården i region Stockholm. Det visar en studie vid Karolinska Institutet som sammanställt resultatet av de första fem årens samarbete kring helgenomsekvensering mellan Karolinska Universitetssjukhuset och SciLifeLab. Arbetet publiceras i tidskriften Genome Medicine och utgör en grund för den framväxande precisionsmedicinen.

– Vi har etablerat ett arbetssätt där sjukhus och universitet samarbetar för att analysera patienters hela arvsmassa i syfte att hitta genetiska förklaringar till olika sjukdomar. Detta är ett exempel på hur precisionsmedicin kan användas för att ställa diagnos och skräddarsy behandling för enskilda patienter, säger studiens förstaförfattare Henrik Stranneheim, forskare vid institutionen för molekylär medicin och kirurgi, Karolinska Institutet.
Den teknologiska utvecklingen av storskalig helgenomsekvensering, dvs sekvensering av en individs hela genuppsättning, har utvecklats snabbt det senaste årtiondet. Trots det är det få kliniker i världen som rutinmässigt använder teknologin.
Hittade sjukdomsorsakande mutationer
För drygt fem år sedan startades centret Genomic Medicine Center Karolinska-Rare Diseases (GMCK-RD) av Karolinska Universitetslaboratoriet och enheten Clinical Genomics på SciLifeLab, där forskare från bland annat Karolinska Institutet och KTH är verksamma. Centret utförde under de första fem åren genanalyser på fler än 3 219 patienter, vilket ledde till klinisk diagnos för fler än 1 287 patienter (40 procent) med sällsynta sjukdomar. Resultaten beskrivs i den studie som nu publicerats.
Totalt hittade forskarna sjukdomsorsakande mutationer i mer än 750 olika gener. Sjutton helt nya sjukdomsgener upptäcktes också. Fynden har i vissa fall gjort det möjligt att individanpassa behandling för patienter med exempelvis medfödda metabola sjukdomar, sällsynta epilepsier och primära immunbrister.

– Klinisk helgenomsekvensering har haft en enorm betydelse inom området sällsynta sjukdomar. Använt på rätt sätt, riktat mot varje patients individuella sjukdomsbild, kan nya grupper av patienter få rätt diagnos och behandling på ett sätt som inte tidigare var möjligt, säger Anna Wedell, professor vid institutionen för molekylär medicin och kirurgi, Karolinska Institutet, och en av studiens korresponderande författare.
Egenutvecklad modell
En stor utmaning vid helgenomsekvensering är att hantera och tolka alla miljontals genvarianter som existerar i varje individ. Centret har därför utvecklat en modell där man först analyserar de gener som brukar innehålla sjukdomsorsakande mutationer utifrån patienternas symtom. Detta innebär att läkarna har en viktig roll i att styra vilka genanalyser ska göras först.
Om de första analyserna inte ger något resultat breddas analysen till fler genpaneler tills en diagnos kan säkerställas och/eller hela genomet sekvenserats. Denna process har även lett till att flera tidigare okända sjukdomsgener har identifierats, vilket gett nya möjligheter att klarlägga sjukdomsmekanismer på djupet, enligt forskarna.
Nu pågår ett omfattande arbete med att implementera liknande arbetssätt på en bredare front inom den svenska hälso- och sjukvården. Bland annat har Karolinska Institutet och Karolinska Universitetssjukhuset nyligen inrättat ett gemensamt precisionsmedicinskt centrum (PMCK) som ska konsolidera och bredda samarbetet kring precisionsmedicin.

– För att lyckas med precisionsmedicin är ett multidisciplinärt samarbete över gränserna mellan sjukvården och akademin helt nödvändigt. Genom dessa initiativ kombinerar vi klinisk kompetens med bioinformatiska verktyg och tillsammans levererar träffsäkra diagnoser och individualiserade behandlingar, säger studiens andra korresponderande författare Anna Lindstrand, professor vid institutionen för molekylär medicin och kirurgi, och överläkare vid avdelningen för klinisk genetik, Karolinska Universitetssjukhuset.
Forskningen har finansierats av Region Stockholm, Vetenskapsrådet, Hjärnfonden, Karolinska Institutet, Knut & Alice Wallenbergs stiftelse och Forskningsrådet i Norge.
Publikation
“Integration of whole genome sequencing into a health care setting: High diagnostic rates across multiple clinical entities in 3219 rare disease patients,” Henrik Stranneheim, Kristina Lagerstedt-Robinson, Måns Magnusson, Malin Kvarnung, Daniel Nilsson, Nicole Lesko, Martin Engvall, Britt-Marie Anderlid, Henrik Arnell, Carolina Backman Johansson, Michela Barbaro, Erik Björck, Helene Bruhn, Jesper Eisfeldt, Cristoph Freyer, Giedre Grigelioniene, Peter Gustavsson, Anna Hammarsjö, Maritta Hellström-Pigg, Erik Iwarsson, Anders Jemt, Mikael Laaksonen, Sara Lind Enoksson, Helena Malmgren, Karin Naess, Magnus Nordenskjöld, Mikael Oscarson, Maria Pettersson, Chiara Rasi, Adam Rosenbaum, Ellika Sahlin, Eliane Sardh, Tommy Stödberg, Bianca Tesi, Emma Tham, Håkan Thonberg, Virpi Töhönen, Ulrika von Döbeln, Daphne Vassiliou, Sofie Vonlanthen, Ann-Charlotte Wikström, Josephine Wincent, Ola Winqvist, Anna Wredenberg, Sofia Ygberg, Rolf H Zetterström, Per Marits, Maria Johansson Soller, Ann Nordgren, Valtteri Wirta, Anna Lindstrand, Anna Wedell, Genome Medicine, online 17 mars, 2021, doi: 10.1186/s13073-021-00855-5
