Viktigt framsteg för forskningen om framtidens läkemedel
En stor andel av alla läkemedel utövar sin effekt via de membran som omger och finns inuti koppens celler. Nu har forskare vid Karolinska Institutet kunnat kartlägga strukturen och mekanismen bakom ett membranenzym som bland annat bidrar till kronisk inflammation och cancer. Studien som publicerats i tidskriften Nature Communications kan få betydelse för utvecklingen av nya läkemedel mot flera sjukdomar.
Kroppens alla celler omges av ett yttre fettrikt membran. Även cellernas motsvarighet till organ, organellerna, är inneslutna av membran. I cellernas yttre och inre membran ligger proteiner inbäddade som reglerar ett stort antal viktiga cellfunktioner. Upp till hälften av alla läkemedel utövar sin verkan på membranproteiner, som till exempel kan vara enzymer, receptorer, eller transportörer.
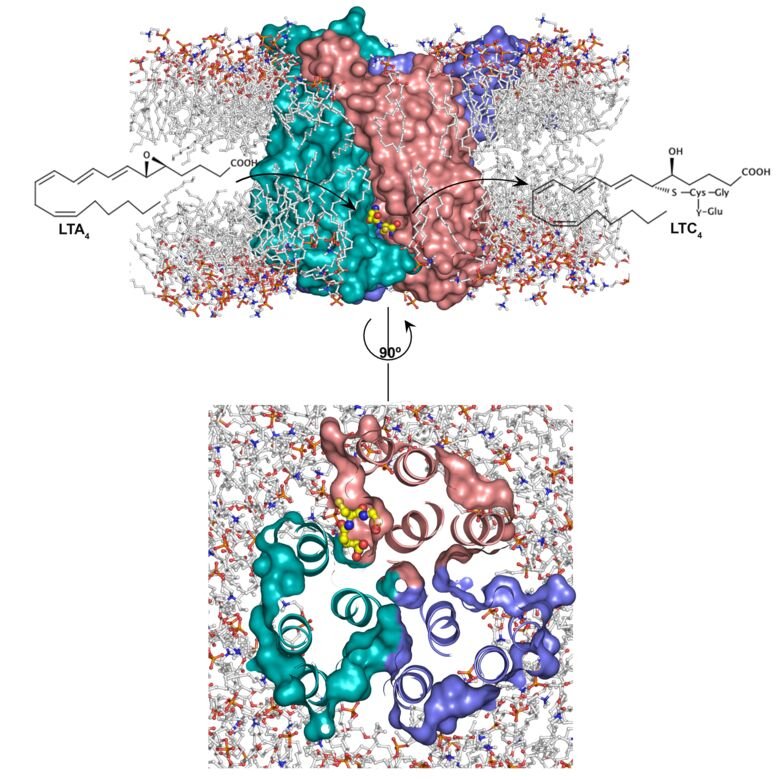
Tre aktiva enheter
Nu har forskare vid Karolinska Institutet med hjälp av röntgenkristallografi, molekylär dynamiksimulering och biokemisk teknik kunnat bestämma den tredimensionella strukturen och mekanismen för ett viktigt enzym inbäddat i cellkärnans membran.
Membranenzymet MGST2, mikrosomalt glutationtransferas typ 2, är motorn i en biokemisk process som ger upphov till så kallad oxidativ stress och bildning av syreradikaler med åtföljande skador på DNA och celldöd.
– Membranproteiner är svåra att studera och det är roligt och spännande att vi lyckats bestämma röntgenstrukturen för MGST2 i hög upplösning. Studien visar bland annat att MGST2 består av tre funktionella enheter som regleras på ett ovanligt sofistikerat sätt. De tre enheterna deltar i sinsemellan koordinerade rörelser så att de turas om att utföra enzymets funktion med en enhet aktiv åt gången, säger Madhuranayaki Thulasingam, forskare vid institutionen för medicinsk biokemi och biofysik, Karolinska Institutet och studiens försteförfattare.
MGST2 tillhör en större familj av enzymer som styr bildning av prostaglandiner och leukotriener, signalmolekyler som styr feber, smärta och inflammation i luftvägar, leder, hjärta och kärl.
Viktig grupp för läkemedelsutveckling

Resultaten ger betydelsefull information om den molekylära regleringen av andra medlemmar av enzymfamiljen, varav flera är viktiga mål för läkemedelsutveckling.
– Vi hoppas att våra resultat skall bidra till utveckling av läkemedel mot ett flertal tillstånd som utmärks av förhöjd produktion av syreradikaler och celldöd såsom kronisk inflammation, cancer och biverkningar av strålning och cytostatika, säger Jesper Z. Haeggström, professor vid institutionen för medicinsk biokemi och biofysik, Karolinska Institutet och huvudansvarig för studien.
Forskningen har finansierats av Vetenskapsrådet, Novo Nordisk Fonden och Karolinska Institutet. Det finns inga rapporterade intressekonflikter.
Publikation
“Crystal structures of human MGST2 reveal synchronized conformational changes regulating catalysis”. Madhuranayaki Thulasingam, Laura Orellana, Emmanuel Nji, Shabbir Ahmad, Agnes Rinaldo-Matthis, Jesper Z. Haeggström. Nature Communications, online 19 mars 2021, doi: 10.1038/s41467-021-21924-8.
