Hjärnavbildning kan förutse försämringar i minnet vid alzheimer

Forskare vid Karolinska Institutet har i en ny studie avbildat proteinet tau i hjärnan hos levande patienter med Alzheimers sjukdom. Mängden och spridningen av tau visade sig kunna förutse hur minnet kommer att utvecklas i framtiden. Hjärnavbildning för att mäta tau kan vara användbar både för att förbättra diagnostiken och för att utveckla mer effektiva behandlingar, enligt forskarna. Studien publiceras i tidskriften Molecular Psychiatry.

Alzheimers sjukdom, den vanligaste demenssjukdomen, kan orsakas av ansamlingar av proteiner i hjärnan som i sin tur leder till skador på nervcellerna och ger minnessvårigheter. Sjukdomsförloppet ser dock olika ut hos olika patienter vilket gör det svårt att förutse hur symtomen för varje enskild individ kommer att utvecklas. För runt 30–50 procent av patienterna kan tillståndet vara stabilt under många år, särskilt i sjukdomens tidiga stadier, medan andra försämras snabbt.
– Moderna hjärnavbildningstekniker erbjuder nya möjligheter att kunna förutse sjukdomsförloppet. Detta har stor betydelse både för att underlätta diagnostisering och optimera vårdinsatser för den enskilda patienten och för utvecklingen av läkemedel, säger studiens försteförfattare Konstantinos Chiotis, läkare och forskare vid institutionen för neurobiologi, vårdvetenskap och samhälle, Karolinska Institutet.
KI-forskarna har under handledning av professor Agneta Nordberg tidigare visat att metoden positronemissionstomografi (PET) kan användas för att avbilda spridningen av proteinet tau i hjärnan hos levande individer. Ansamlingar av tau kopplas till Alzheimers sjukdom.
Följdes i över fyra år
I den aktuella studien genomgick 20 patienter en omfattande utredning med alla befintliga kliniska markörer för Alzheimers sjukdom på Kognitiva Mottagningen vid Karolinska Universitetssjukhuset. De fick också genomgå positronemissionstomografi för att avbilda tau-protein i hjärnan. Forskarna följde sedan patienterna i över fyra år för att bedöma om deras kognitiva funktioner försämrades med tiden. Syftet var att undersöka om mängden tau kunde förutse vilka patienter som skulle få ett långsamt eller snabbt sjukdomsförlopp.
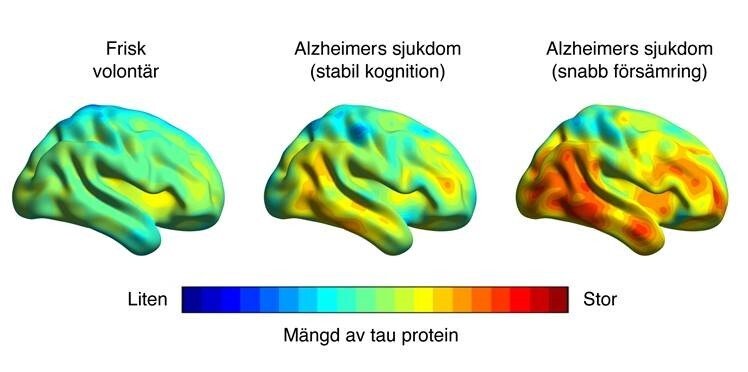
De patienter som hade en liten mängd tau-protein initialt visade stabil funktion under uppföljningen, medan patienter med stora mängder tau försämrades snabbt kognitivt. Mängden och spridningen av tau-protein i hjärnan kunde skilja de olika patientgrupperna åt med en precision på över 95 procent, medan precisionen av de befintliga kliniska markörerna var som högst 77 procent. Den exakta mängden av tau-protein överensstämde även väl med den exakta graden av försämring på den kliniska skalan. Denna skala används rutinmässigt på de flesta mottagningar som mäter den kognitiva funktionen hos patienter med minnesbesvär.
Kan få betydelse för läkemedelsutveckling

– Våra resultat antyder att tau-proteinet har stor påverkan på hjärnans kognitiva funktion. Det innebär att läkemedel som riktar sig mot ansamlingar av tau skulle kunna ha bättre chanser att förändra sjukdomsförloppet än de behandlingar som hittills testats och misslyckats, säger Agneta Nordberg, som lett studien.
Forskningen finansierades av Stiftelsen för Strategisk Forskning, Vetenskapsrådet, Region Stockholm (ALF-medel), Svenska Sällskapet för Medicinsk Forskning, Loo och Hans Ostermans stiftelse för medicinsk forskning, Stiftelsen för ålderssjukdomar vid Karolinska Institutet, Magnus Bergvalls Stiftelse, Tore Nilsons Stiftelse för Medicinsk Forskning, Stiftelsen Sigurd och Elsa Goljes Minne, Eva och Oscar Ahréns Stiftelse, Stiftelsen För Gamla Tjänarinnor, Axel Linders Stiftelse, Åhlén-Stiftelsen, Gun och Bertil Stohnes Stiftelse, KI:s fonder, Hjärnfonden, Alzheimerfonden, Demensfonden, Demensförbundet och EU:s forskningsprojekt INMiND.
Publikation
“[18F]THK5317 imaging as a tool for predicting prospective cognitive decline in Alzheimer’s disease”. Konstantinos Chiotis, Irina Savitcheva, Konstantinos Poulakis, Laure Saint-Aubert, Anders Wall, Gunnar Antoni, Agneta Nordberg. Molecular Psychiatry, online 3 juli 2020, doi: 10.1038/s41380-020-0815-4.
